乙肝标志物
乙肝病毒免疫标志物
1. 简述乙肝病毒免疫标志物的临床意义?
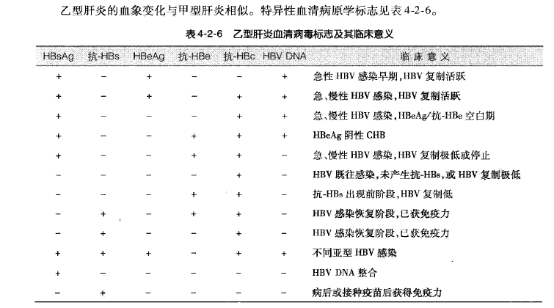
传统HBV血清学标志物包括HBsAg、抗-HBs、HBeAg、抗-HBe、抗-HBc和抗-HBcIgM。
HBsAg一般在感染早期出现,血清HBsAg可由cccDNA转录的mRNA翻译产生,也可由整合入宿主基因组的HBVDNA序列转录翻译而来。HBsAg阳性表示HBV感染,其阳性是HBV感染的主要标志。但不能反映病毒复制情况及预后,其定量检测可用于预测疾病进展、抗病毒疗效和预后。HBsAg定量检测已在临床中被广泛应用,其水平可反映疾病分期与疾病进展风险,也可用于指导重组人干扰素和聚乙二醇干扰素α(peginterferon-α,Peg-IFN-α)治疗。
HBsAg阳性者可以分为两种,如HBe-Ag、HBVDNA阳性为慢性HBV携带者(3-6月复查),而HBe-Ag、HBVDNA阴性为非活动性乙肝表面抗原携带者(6个月复查)。区分的目的,分类便于管理。避免两种倾向:不随访,过度治疗。阴性不能排除乙肝病毒感染。
慢性HBV携带状态:患者多处于免疫耐受期,年龄较轻,HBVDNA定量水平(通常>2×107IU/ml)较高,血清HBsAg水平(通常>1×104IU/ml)较高、HBeAg阳性,但血清ALT和AST持续正常(1年内连续随访3次,每次至少间隔3个月),肝脏组织病理学检查无明显炎症坏死或纤维化。在未行组织病理学检查的情况下,应结合年龄、病毒水平、HBsAg水平、肝纤维化无创检查和影像学检查等综合判定。
非活动性HBsAg携带状态:患者血清HBsAg阳性、HBeAg阴性、抗-HBe阳性,HBVDNA阴性(未检出),HBsAg<1000IU/ml,ALT和AST持续正常(1年内连续随访3次以上,每次至少间隔3个月);影像学检查无肝硬化征象,肝组织学检查显示组织活动指数(histologicalactivityindex,HAI)评分<4或根据其他半定量计分系统判定病变轻微。
复习题 HBsAg阳性者可以分为两种,两者有何不同?
HBsAg携带者 | 慢性HBV携带者 | 非活动性HBsAg携带者 |
HBe-Ag | 阳性 | 阴性 |
HBV-DNA | 阳性 | 阴性 |
传染性 | 强 | 低 |
复查 | 3-6月 | 6月 |
相同 | HBsAg连续阳性3次/年(间隔3月) 转氨酶正常 肝组织检查无病变或病变轻微 | |
对于HBsAg阳性者随访检查项目包括肝功能、HBVDNA、AFP及肝脏彩超,如HBVDNA应做肝穿刺检查。
建议肝穿刺检查 40岁以上 乙肝家族史 转氨酶在正常高限 B超提示肝脏弥漫性病变或脾脏增大者 | 抗病毒治疗: 肝穿刺结果炎症分级G≥2,或有明显纤维化 发现ALT升高超过正常上限2倍,同时HBVDNA阳性,排除药物及酒精所致肝功能异常 |
抗HBs为保护性抗体,其阳性表示对HBV有免疫力。抗HBs阳性为感染恢复的标志及接种乙型肝炎病毒疫苗。
抗HBs 感染恢复 注射乙肝疫苗(获得免疫力,要求>=10mIU/ml才有保护作用) 血清转换期 |
HBe-Ag提示HBV复制,也在感染早期出现。抗-HBe阳性是既往感染的标志。半定量单位为PEIU/ml,为PaulEhrlichInstitute(PEI)的标准单位
根据HBe-Ag是否阳性把慢性乙肝感染者分为HBe-Ag阳性慢性乙肝感染和HBe-Ag阴性慢性乙肝感染。
复习题 慢性乙肝感染者分为HBe-Ag阳性慢性乙肝感染和HBe-Ag阴性慢性乙肝感染,两者有何不同?
慢性乙肝感染 | HBe-Ag阳性CHB | HBe-Ag阴性 |
乙肝标志物 | HBsAg+、HBeAg+
| HBsAg阳性、HBeAg 持续阴性,多同时伴有抗 -HBe阳性
|
HBV-DNA | 高 | 低<20000,大多在2000以下 |
ALT | 正常上限范围内 持续或反复异常 | 持续或反复异常 |
肝活检 | 异常有明显炎症坏死,或肝组织学 | 明显坏死性炎症活动和轻度纤维化 |
无创指标 | 提示有明显纤维化 (≥F2) | 有明显纤维化 (≥F2)。
|
HBcAg一般不能检出,其抗体阳性提示既往感染或现症感染。抗-HBc IgM阳性,为急性乙型肝炎,滴度更高,而慢性HBV感染急性发作也可呈低水平阳性;抗-HBc总抗体主要是抗-HBcIgG,只要感染过HBV,不论病毒是否被清除,此抗体通常为阳性。IgG阳性为慢性感染或IgM和IgG同时阳性提示慢性病毒性感染急性发作。
复习题 HBsAg与抗HBs同时阳性有哪些原因?
同时出现阳性,发生率5%,可见于以下情况:
将发生血清学转换,即从HBsAg转变为抗HBs;抗HBs针对另一种血清亚型的HBsAg的抗体,与HBsAg的抗体不是同一种抗体(即抗体与HBsAg不匹配);
HBV S基因的“a”表位发生变异。
HBsAg抗原性较为复杂有多个抗原表位:“a”和至少两个亚型“d/y”和“w/r”,有十个亚型,主要为adw、adr、ayw、ayr。当a表位发生突变时,将导致针对抗原的抗体也发生变化。
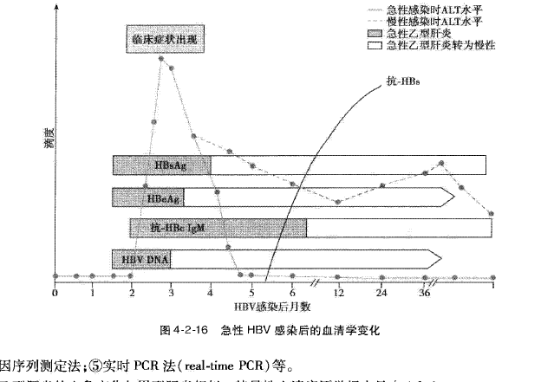
2.HBV-DNA
HBVDNA定量:主要用于评估HBV感染者病毒复制水平,是抗病毒治疗适应证选择及疗效判断的重要指标。不仅用于HBV感染的诊断,也用于疗效观察。HBVDNA定量采用实时定量聚合酶链反应法(polymerasechainreaction,PCR),随着检测试剂灵敏度的提高,目前定量下限可达10~20IU/ml甚至更低。出现比较早,检测结果用copy/ml表示,国际上采用IU/mL(1IU=5.6copy)。
对筛查出的HBsAg阳性者,以及已经开始抗病毒治疗的CHB患者,采用高灵敏的实时定量PCR方法检测HBVDNA,有助于检出低病毒载量的患者,以便尽早开始抗病毒治疗或及时调整治疗方案。
必要做基因分型和耐药性检测。HBV基因分型:目前,可鉴定出至少9种基因型和1种未定型,一些基因型可分数种基因亚型。检测HBV基因型有助于预测干扰素疗效,判断疾病预后。在慢性持续性感染过程中发生自然变异,也可因抗病毒药物治疗诱导而产生病毒变异,均可导致对抗病毒药物敏感性下降。耐药突变株检测HBV有助于抗病毒治疗的选择。
对HBsAg阳性者,包括正在接受抗病毒治疗的CHB患者,应尽可能采用高灵敏且检测线性范围大的HBVDNA检测方法(定量下限为10~20IU/ml)
HBV 感染者的传染性高低主要取决于血液中 HBV DNA 水平, 与血清丙氨酸 转氨酶( ALT) 、天冬氨酸转氨酶 (AST)和胆红素水平无关。
3.HBV新型标志物检测?
HBVRNA定量 乙型肝炎核心相关抗原(hepatitisBcore-relatedantigen,HBcrAg) 抗-HBc定量
|
HBVRNA定量:被认为与肝细胞内cccDNA转录活性有关。有研究探讨了其与HBVDNA或乙型肝炎核心相关抗原(hepatitisBcore-relatedantigen,HBcrAg)联合在预测NAs停药后复发风险的应用;是否可以作为替代指标反映NAs治疗中(病毒学抑制)或HBsAg消失后肝内病毒的转录活性仍有待探索]。
HBcrAg:是一种包含HBcAg、HBeAg、p22蛋白质的复合标志物,与肝细胞内cccDNA转录活性有关。有研究探讨了其在区分疾病分期及预测Peg-IFN-α抗病毒疗效、NAs停药后复发和HBsAg消失、HCC发生风险等方面的应用。
抗-HBc定量
有研究显示,在未经治疗慢性HBV感染的患者中,ALT正常或<80IU/L者肝组织炎症程度和抗-HBc定量水平呈显著正相关;治疗后抗-HBc定量水平的下降与肝组织炎症程度减轻同步变化。抗-HBc定量水平和肝组织纤维化程度正相关。此外,有研究讨论了其在区分疾病分期、预测Peg-IFN-α和NAs抗病毒疗效、停药后复发、预测慢加急性肝衰竭(acute-on-chronicliverfailure,ACLF)临床预后等方面的应用。
4.隐匿性HBV感染(OBI)?
患者血清HBsAg阴性,但血清和/或肝组织中HBVDNA阳性。在OBI患者中,80%可有血清抗-HBs、抗-HBe和/或抗-HBc阳性,称为血清阳性OBI;但有1%~20%的OBI患者所有HBV血清学标志物均为阴性,故称为血清阴性OBI。
早期研究认为0B1形成可能的原因有:①e抗原血清学转换后,在长期的病毒无复制期检测不到HBsAg;②由于HBV基因发生变异,导致HBsAg无法合成或无法通过血清学检测方法检测;③其他病毒(HDV、HCV)合并感染干扰HBV的复制。
随着分子生物学研究的进展,目前认为HBsAg阴性的原因主要以下几个方面:
1.HBV基因变异HBV是双链环形DNA病毒,其核酸长链带有全部病毒蛋白编码,主要有4个开放可读框,包括编码外膜蛋白的前S/S基因区、编码壳蛋白的前C/C基因区、调节病毒基因转录水平的x基因区和编码聚合酶的P基因区。这些区域都可能发生变异,其中前S/S区的变异,可影响HBV膜蛋白的表达,使HBsAg检出阴性。
2.HBV感染可以诱导宿主基因组甲基化,与宿主细胞周期调控、信号转导、DNA损伤修复和免疫调节等方面的改变相关;另一方面HBVDNA也可被宿主肝细胞甲基化,使病毒复制减弱病毒蛋白表达下调。当HBV侵入人的肝细胞时,在细胞质中脱去核壳,在宿主细胞的DNA聚合酶作用下形成超螺旋结构的共价闭合环状DNA。HBV共价闭合环状DNA甲基化导致病毒蛋白及HBV前基因组RNA的量减少,而前基因组RNA的合成是HBV复制的起始步骤。
4.PBMC感染HBVPBMC能够受到HBV和其他嗜肝DNA病毒的感染,PBMC中存在的HBV可能是OBI的原因之一。经过治疗后血清病毒指标(HBsAg)转阴的患者,PBMC中仍可检测出HBV DNA。在肝移植时,接受了血清HBsAg阴性和抗HBcAb阳性的供体,但肝脏和PBMC中仍可检测到HBVDNA。
5.宿主免疫应答异常宿主的免疫监督在OBI的形成中起重要作用。HBV在宿主细胞中的表达与宿主自身免疫因素密切相关。一方面,宿主免疫应答低下,清除HBV能力下降是OBI发生的一个因素;另一方面,所有诱导免疫抑制的情况可以引起OBI的再激活,并有典型HBV感染的血清学标志出现。此外,感染时间过长也是原因之一。调查发现,OBI患者中,老年人比例较高,这可能与老年人免疫水平相对较低及感染HBV时间较长有关,血液中HBsAg水平随感染时间延长而下降。
5.基因组及基因组突变
HBV为为嗜肝DNA病毒科正嗜肝DNA病毒属的一员,HBV 通过肝细胞膜上的钠离子-牛磺胆酸-协同转运蛋白( NTCP)作为受体进入肝细胞。现在发现也可在肝外组织复制,主要为外周血单个核细胞,一般认为在外周血单个核细胞内潜伏的HBV是肝移植后HBV再感染的主要来源。在血清中有三种形式的病毒相关颗粒,在血液中主要以小球形颗粒最多,含有HBVDNA的Dane颗粒较少。
HBV基因组为部分环状双链DNA,全长3182kb,其负链含四个开放性读框架,其复制过程极为复杂且特殊。编码 HBsAg、HBcAg、HBeAg、病毒聚合酶和 HBx 蛋白。在细胞核内以负链DNA 为模板形成共价闭合环状 DNA(cccDNA)。 cccDNA 难以彻底清除,是导致慢性感染的重要机制之一。 以 cccDNA 为模板转录而成的前基因组RNA (pgRNA) 可释放入外周血,血清 HBV RNA 被认为与肝细胞内 cccDNA 转录活性有关。 HBV 可整合至宿主肝细胞基因组中,HBV 整合被认为与 HBsAg 持续表达和HCC 发生密切相关。 HBV至少有9 种( A 型至 I 型)基 因型和 1 种未定基因型( J 型) 。 我国以B 基因型和 C 基因型为主。 HBV 基因型与疾病进展和干扰素 α 治疗应答有关,鉴定基因型有助于治疗药物的选择,A型对α-干扰素治疗的应答率高于B、C、D。不影响核苷(酸)类似物的疗效。 HBV 突变率较高,逆转录酶区的突变多与核苷(酸)类似 物[ ,NAs]耐药有关,前 S / S 区、基本核 心启动子区、前C / C 区的部分突变可能与发生急性肝功能衰竭和 HCC 有关。HBV基因组易变异,决定HBV优势株的构成。
基因组分区 | S | C(前C基因和C基因) | P | X |
编码 | 前S1 前S2 S蛋白(HBsAg) | C基因编码HBcAg 前C基因前起始密码子连续编码前基因及C基因形成HBeAg前体,后被水解形成HBeAg
| DNA聚合酶 | HBxAg 与HBcAg在肝细胞分布一致 |
S基因突变导致隐匿性HBV感染,HBsAg隐性,而HBV低水平复制。在疫苗诱导抗体的诱导下,出现S基因突变,将出现免疫逃避,发生HBV突破性感染,影响免疫接种效果,但还不足以对疫苗接种计划构成威胁。也影响被动免疫疗效。
前C/C基因变异是形成HBeAg阴性的慢性乙肝病毒肝炎的主要原因。HBV逆转录酶区变异是导致抗病毒治疗耐药的原因之一。
复习题 DNA聚合酶的特性?
1. 具有DNA指导的DNA多聚酶
2. RNA指导的DNA多聚酶
3. RNA酶H活性
4. 缺乏校对功能,是基因组易发生变异的原因
6.乙型肝炎疫苗全程需接种3 剂, 即接种第 1 剂疫苗后,在第 1 个月和第 6 个月时注射第 2 剂和第3 剂。 接种乙型肝炎疫苗越早越好。 危重症新生儿,如超低体质量儿( <1 000 g) 、严重出生缺陷、重度窒息、呼吸窘迫综合征等
应在生命体征平稳后,尽早接种第 1 剂乙型肝炎疫苗。
乙型肝炎疫苗全程接种:按照 0、1、6 个月的程序 加速疫苗接种程序:0、1、2 个月程序 |
新生儿 不论母亲 HBsAg阳性与否 ,重组酵母乙型肝炎疫苗每剂次10 μg HBsAg 阳性母亲的新生儿 在不同部位接种乙型肝炎疫苗 在出生后12 h 内尽早注射乙型肝炎免疫球蛋白(HBIG) 成人 20 μg 重组酵母乙型肝炎疫苗或 20μg重组中国仓鼠卵巢(Chinese hamster ovary, CHO)细胞乙型肝炎疫苗 免疫低下 应增加疫苗的接种剂量 (如 60 μg)或剂次 妊娠期间 接种乙型肝炎疫苗是安全的 |
新生儿接种部位为上臂外侧三角肌或大腿前外侧中部肌内注射;儿童和成人为上臂三角肌中部肌内注射。 即使进行主动和被动免疫,仍有约 5% ~ 10% HBeAg 阳性且 HBV DNA 高水平母亲所生婴儿发生 HBV 感染,其危险因素包括母亲HBeAg 阳性、 HBV DNA 高载量、 准种特征和HBx 基因特征 。 HBeAg 阳性母亲或 7 月龄时低抗-HBs 水平的儿童,应在 2 岁前及时加强免疫注射,而不要等到其抗-HBs阴转再加强免疫注射。
对免疫功能低下或无应答者,对 0、1、6 个月程序无应答者可再接种 1剂 60 μg 或 3 剂 20 μg 乙型肝炎疫苗,并于完成第 2 次接种程序后 1 ~ 2 个月时检测血清抗-HBs。 如仍无应答,可再接种 1 剂 60 μg 重组酵母乙型肝炎疫苗。 未感染过 HBV 的妇女在妊娠期间也可接种乙型肝炎疫苗。 加速疫苗接种程序已被证明是可行和有效的。
7.意外暴露于HBV者如何处理?
(1)在伤口周围轻轻挤压,排出伤口中的血液,再对伤口用等渗盐水冲洗,然后用消毒液处理 。
(2)应立即检测 HBsAg、 HBV DNA,3 ~ 6 个月后复查 。
(3)如接种过乙型肝炎疫苗并有应答者,且已知抗-HBs阳性(抗-HBs≥10 mIU / ml) 者,可不再注射 HBIG 或乙型肝炎疫苗。
如未接种过乙型肝炎疫苗,或虽接种过乙型肝炎疫苗,但抗-HBs<10 mIU / ml 或抗-HBs 水平不详者,应立即注射 HBIG 200 ~ 400 IU,同时在不同部位接种 1 剂乙型肝炎疫苗(20 μg) ,于 1 个月和 6 个月后分别接种第 2 剂和第 3 剂乙型肝炎疫苗(20 μg) 。